Pexidartinib在腫瘤免疫微環境、腫瘤抑制、神經免疫上的應用研究_abio生物試劑品牌網
一、 Pexidartinib ( PLX3397 ) 的作用機制
CSF-1R在多種細胞的生長、存活、分化及功能調節中發揮著關鍵作用。在正常生理狀態下,CSF-1與其受體CSF-1R結合,激活下游一系列信號轉導途徑,包括RAS-MAPK、PI3K-AKT和 JAK-STAT 等通路,進而調控細胞的多種生物學行為。當Pexidartinib(PLX3397,AbMole,M4867)作用于細胞時,它能夠與CSF-1R的ATP結合位點緊密結合,阻斷ATP與受體的結合,從而抑制CSF-1R的磷酸化及后續的信號轉導過程。在一些以巨噬細胞為研究對象的體外實驗中,加入Pexidartinib后,巨噬細胞對CSF-1刺激的響應被削弱,表現為細胞增殖速度減緩,細胞周期相關蛋白的表達發生改變,這充分證明了Pexidartinib對CSF-1R信號通路的有效阻斷 [1]。 KIT和FLT3則在細胞的生長、分化及造血過程中扮演著重要角色。KIT信號通路的異常激活與多種細胞的異常增殖和分化相關,而FLT3的內部串聯重復(ITD)突變在一些血液系統疾病中較為常見,會導致該信號通路的持續激活。Pexidartinib能夠通過抑制KIT和FLT3的激酶活性,阻斷其下游信號轉導。用Pexidartinib處理FLT3突變的細胞系時發現,FLT3下游的STAT5磷酸化水平明顯下降,細胞的增殖能力顯著降低。在一些白血病細胞模型中,Pexidartinib能夠抑制KIT和FLT3的活性,影響細胞內相關信號分子的磷酸化狀態,進而誘導細胞凋亡或改變細胞的分化方向 [2]。此外,Pexidartinib可以通過抑制KIT信號通路,減少相關細胞中BCL-2蛋白的表達,促進細胞凋亡的發生 [2]。 2014年,AbMole的兩款抑制劑分別被西班牙國家心血管研究中心和美國哥倫比亞大學用于動物體內實驗,相關科研成果發表于頂刊 Nature 和 Nature Medicine。
二、 Pexidartinib ( PLX3397 ) 的科研應用
1. Pexidartinib ( PLX3397 ) 用于調節腫瘤免疫微環境
腫瘤免疫微環境(Tumor Immune Microenvironment, TIME)是腫瘤組織內部及周圍由免疫細胞、細胞因子、血管網絡、細胞外基質等共同構成的動態生物環境,其核心特征是免疫抑制(促進腫瘤逃避免疫系統)、參與腫瘤的發生和轉移。巨噬細胞在TIME中主要有兩種形態,即具有抗腫瘤活性的M1型和促進腫瘤生長、轉移及免疫逃逸的M2型。TIME中的CSF-1(集落刺激因子因子1)可促進免疫抑制性M2表型巨噬細胞的募集和分化。許多細胞實驗表明, Pexidartinib (PLX3397,AbMole,M4867 )能夠有效抑制巨噬細胞向M2型極化,并降低腫瘤組織中M2型巨噬細胞的數量。Pexidartinib 處理后,M2型巨噬細胞相關基因如CD206、CCL-2 的 mRNA 表達下降,而M1型巨噬細胞相關基因如IL-1β、iNOS、CD80的 mRNA 表達相對增加。這些結果一致表明,Pexidartinib能夠對腫瘤免疫微環境產生積極的調節作用 [1]。
2. Pexidartinib ( PLX3397 ) 用于急性髓性白血病(AML)的研究
對于FLT3-ITD突變的急性髓性白血病(AML),研究發現FLT3-ITD陽性AML細胞能夠極化M2樣白血病相關巨噬細胞(M2-LAM),并抑制其吞噬活性,而M2-LAM 能通過激活FLT3信號通路保護 AML 細胞免受 FLT3抑制劑的影響。Pexidartinib https://www.abmole.cn/products/pexidartinib.html作為 FLT3/CSF1R 雙重抑制劑,能夠有效抑制M2-LAM,并延長MOLM-13小鼠模型的生存期。此外,也有研究構建了以FLT3配體為識別域的CAR-巨噬細胞,與Pexidartinib聯合使用,在體外實驗中,CAR-巨噬細胞能夠有效吞噬MOLM-13細胞,這為 FLT3-ITD陽性AML 的抑制提供了一種新的、有前景的聯合策略。Pexidartinib在其中發揮了關鍵的調節腫瘤微環境中巨噬細胞功能的作用,與 CAR-巨噬細胞治療協同抑制AML細胞的生長 [3]。
3. Pexidartinib ( PLX3397 ) 用于 多種 腫瘤 的 細胞和動物模型 抑制研究
Pexidartinib (PLX3397,AbMole,M4867 )在多種類型的腫瘤細胞中表現出了強大的抑制活性。例如在卵巢癌的研究中發現,CSF-1R高表達與腫瘤體積增大、淋巴結轉移增多、以及小鼠生存期顯著縮短密切相關。體外實驗中,Pexidartinib能夠有效抑制卵巢癌細胞的增殖,誘導細胞周期停滯在G1期,促進細胞凋亡,抑制克隆形成,減少細胞遷移和侵襲能力。在ID8卵巢癌小鼠模型中,Pexidartinib與紫杉醇聯合使用,顯著抑制了腫瘤生長,減少了腹水生成,并延長了小鼠的生存期 [4]。在黑色素瘤小鼠模型中,Pexidartinib同樣表現出良好的抗腫瘤效果:在B16F10小鼠黑色素瘤模型中,Pexidartinib能夠減少免疫抑制性巨噬細胞在全身和腫瘤局部的積累 [5]。在結直腸癌相關研究中,Pexidartinib 也顯示出對腫瘤生長和轉移的抑制作用,在小鼠結直腸癌腹膜內轉移模型中,使用腫瘤微環境響應性靶向納米顆粒共同遞送表達IL-12基因和 Pexidartinib,實驗組小鼠腹腔腫瘤重量最低,轉移性結節顯著減少 [6]。除了上述細胞和動物模型外,Pexidartinib還能用于骨肉瘤、前列腺腫瘤細胞、結直腸癌等模型的研究 [7]。
4. Pexidartinib ( PLX3397 ) 用于神經免疫學研究
神經免疫系統是中樞神經系統(CNS)維持穩態的核心調控網絡,其異常激活與神經退行性疾病、神經創傷及神經腫瘤的發生發展密切相關。小膠質細胞作為 CNS 內的固有免疫細胞,通過動態調控炎癥反應、突觸修剪和神經修復,在神經免疫過程中扮演關鍵角色。集落刺激因子 1 受體(CSF-1R)信號通路在小膠質細胞的存活、增殖和極化中起決定性作用,而 Pexidartinib (PLX3397,AbMole,M4867 )作為高選擇性CSF-1R酪氨酸激酶抑制劑,通過靶向該通路重塑神經免疫微環境,為神經免疫疾病的機制研究和干預策略提供了新視角 [8]。
三、 范例詳解
Cancer Lett. 2022 Feb 28;527:174-190.
上海交通大學、南京醫科大學的實驗人員在上述研究中探討了三陰性乳腺癌(TNBC)中的 Hippo/YAP 信號通路,及其對腫瘤免疫微環境的調控作用。研究發現Hippo通路與TNBC預后不良及免疫微環境高度相關,其關鍵分子TAZ的高表達會減少CD8陽性T細胞的浸潤、增加腫瘤相關巨噬細胞(TAMs)浸潤,形成免疫抑制微環境。在分子機制上,科研人員發現TAZ通過直接調控IL-34和PD-L1的轉錄,促進TAMs的增殖和遷移,同時抑制T細胞的免疫功能;此外,TAMs分泌的TGF-β1會反促 TAZ 表達,形成正反饋 loop,加劇腫瘤進展。研究團隊還設計并驗證了如下的抑制策略:通過將CSF-1R 抑制劑(Pexidartinib)與PD-L1 抗體聯合使用,可顯著減少TAMs浸潤、增加CD8陽性T細胞的浸潤,逆轉免疫抑制微環境,協同抑制TNBC生長和轉移。在上述實驗中,科研人員使用了由AbMole提供的 Pexidartinib (PLX3397,AbMole,M4867 ) [1] 。
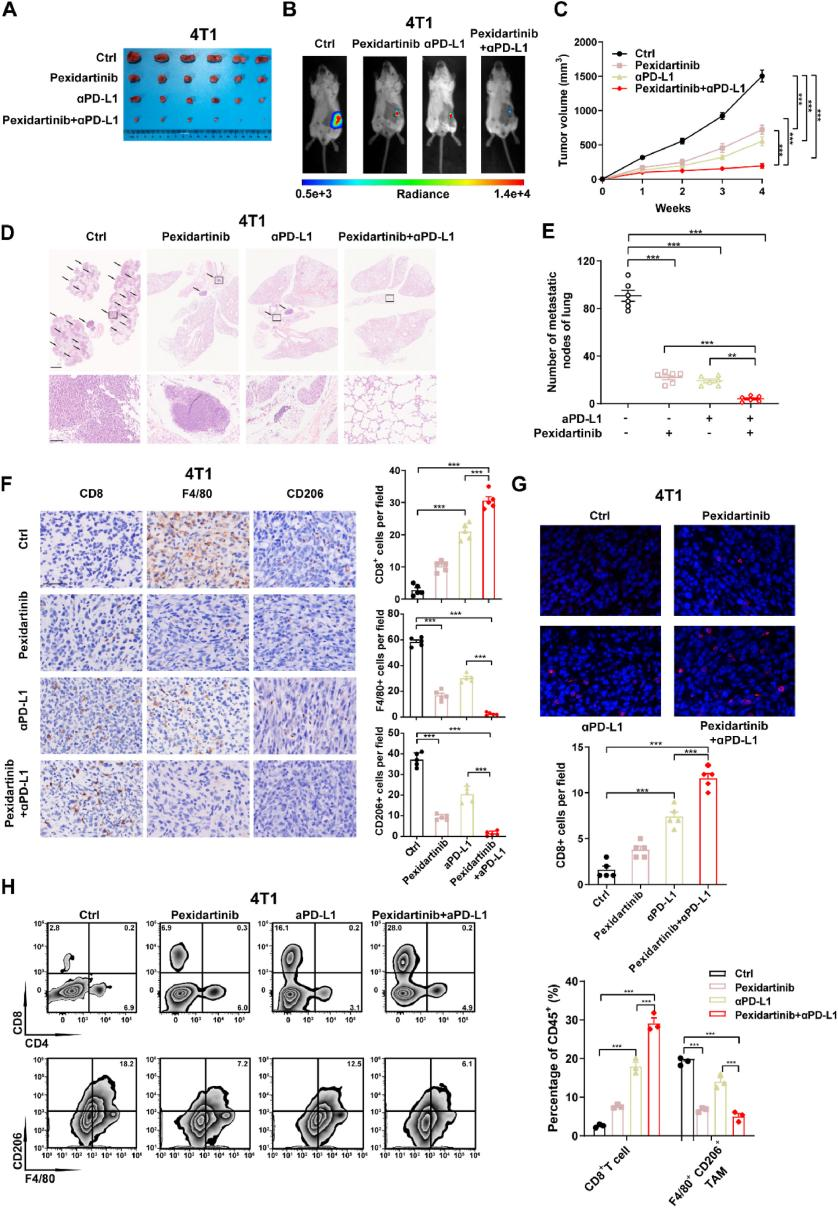
 圖 1. CSF-1R 阻斷通過逆轉免疫抑制腫瘤微環境使 TNBC 對PD-L1抗體敏感
[1]
圖 1. CSF-1R 阻斷通過逆轉免疫抑制腫瘤微環境使 TNBC 對PD-L1抗體敏感
[1]
AbMole是ChemBridge中國區官方指定合作伙伴。

參考文獻及鳴謝
[1] Z. Wang, F. Wang, X. Y. Ding, et al., Hippo/YAP signaling choreographs the tumor immune microenvironment to promote triple negative breast cancer progression via TAZ/IL-34 axis, Cancer letters 527 (2022) 174-190.
[2] A. P. Schade, D. A. Smith, L. M. Klinghoffer, et al., PLX3397, a novel CSF1R, KIT, and FLT3 inhibitor, is active in models of human acute myeloid leukemia, Leukemia 27 (2013) 2218-2227.
[3] J. H. Park, Y. J. Kim, S. H. Lee, et al., FLT3 ligand-targeted CAR-macrophages combined with PLX3397 enhance phagocytosis and anti-leukemic activity in FLT3-ITD+ AML, Blood advances 5 (2021) 3452-3465.
[4] Y. Liu, H. Zhang, X. Li, et al., CSF-1R inhibitor PLX3397 enhances paclitaxel efficacy in ovarian cancer by reprogramming tumor-associated macrophages, Journal of experimental & clinical cancer research 40 (2021) 324.
[5] S. A. Condeelis, J. M. Pollard, Macrophages and metastasis: implications for new cancer therapies, Nature reviews cancer 16 (2016) 709-723.
[6] X. Zhang, L. Chen, Y. Wang, et al., Tumor microenvironment-responsive nanoparticles co-delivering IL-12 plasmid and PLX3397 for combinatorial immunotherapy of colorectal cancer, Journal of controlled release 332 (2021) 600-613.
[7] W. D. Tap, H. Gelderblom, E. Palmerini, et al., Pexidartinib versus placebo for advanced tenosynovial giant cell tumour (ENLIVEN): a randomised phase 3 trial, Lancet 394 (2019) 478-487.
[8] M. A. Colonna, R. Butovsky, Microglia function in the central nervous system during health and neurodegeneration, Annual review of immunology 35 (2017) 441-468.
本站“ABIO生物試劑品牌網”圖片文字來自互聯網
如果有侵權請聯系微信: nanhu9181 處理,感謝~


