陰離子層析(AEX)的病毒去除表現以及影響因素_abio生物試劑品牌網
病毒污染是使用源自哺乳動物細胞系的生物技術產品的潛在風險。生產過程中,無論處于臨床前非GMP、臨床GMP或商業化階段,均可能受到內源性或外源性病毒的污染,對患者安全構成嚴重威脅。據統計,過去36年間共報告了26起哺乳動物細胞培養物的病毒污染事件,其發生在產品生命周期的所有階段。因此,確保產品病毒安全性是行業監管與工藝開發的核心關注點。
為了保證這些產品在潛在病毒污染方面的安全性,監管機構要求進行病毒清除研究,以評估純化過程清除內源性和外源性病毒的能力。一般來說,下游工藝減少病毒是通過柱層析和專用的病毒去除步驟(即低pH值孵育、去污劑處理和納濾)來實現的。本文將簡述陰離子層析(Anion exchange chromatography, AEX)病毒去除效果及影響因素。
AEX病毒去除機理與能力在下游純化工藝中,層析步驟除有效去除工藝相關雜質和產品相關雜質外,亦是重要的病毒清除單元操作。其中,AEX常被證明是病毒清除最為關鍵的步驟。 AEX病毒去除機理
AEX用于抗體類項目純化時,主要采用兩種模式:
? 流穿模式 (Flow Through Mode, FT):此模式利用目標單抗與模型病毒等電點(PI)的差異。多數單抗pI較高,在適宜的緩沖液條件下(pH 7.0~8.5,低電導率),單抗因帶正電荷而流穿;而模型病毒(如X-MuLV pI~5.8, MVM pI~6.2)在此條件下帶負電荷,通過與填料帶正電荷的配基發生靜電吸附而被去除。
? 結合-洗脫模式 (Bind and Elute Mode, B/E):此模式則利用單抗與病毒在結合力強度上的差異。在特定條件下,單抗和病毒均結合至填料上,隨后通過改變洗脫條件,選擇性地洗脫單抗,而病毒仍保留在填料上。
AEX色譜病毒去除能力大量數據庫數據顯示,FT模式AEX能有效去除包膜病毒和非包膜病毒,統計數據表明(如Fig.1):
? 約70%的AEX應用采用FT模式,約30%采用B/E模式。
? FT模式對兩種病毒表現出較高的穩健性,且批次間變異性較低。
? B/E模式對兩種病毒的清除能力呈現更高的批次間變異性。
? 兩種模式下細小病毒批次間變異性均大于逆轉錄病毒。
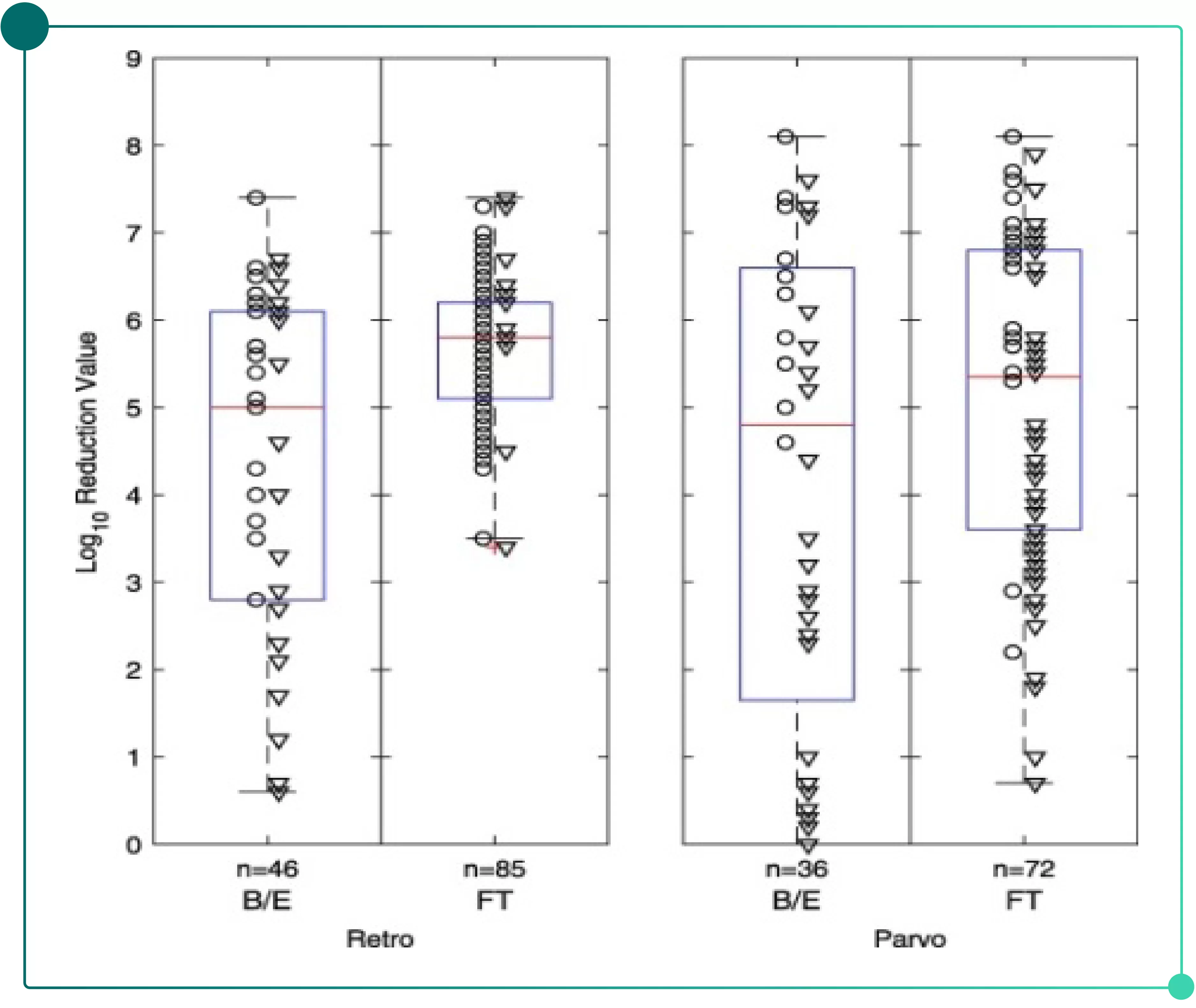 Fig.1 陰離子交換層析對逆轉錄病毒和細小病毒的去除能力總結(FDA數據庫統計)
Fig.1 陰離子交換層析對逆轉錄病毒和細小病毒的去除能力總結(FDA數據庫統計)
復合模式陰離子層析病毒去除能力
復合模式層析填料同時具有離子交換與疏水相互作用等多種作用力,這種多模式機制賦予了其獨特的優勢:
? 增強緩沖液的兼容性:可在更寬的pH值和電導率范圍內有效運行。
? 更穩健的病毒清除:如Fig.2所示,與單一模式AEX相比,復合模式AEX在高鹽條件下仍能維持優異的細小病毒去除效能(在高鹽區仍保持較高LRV)。
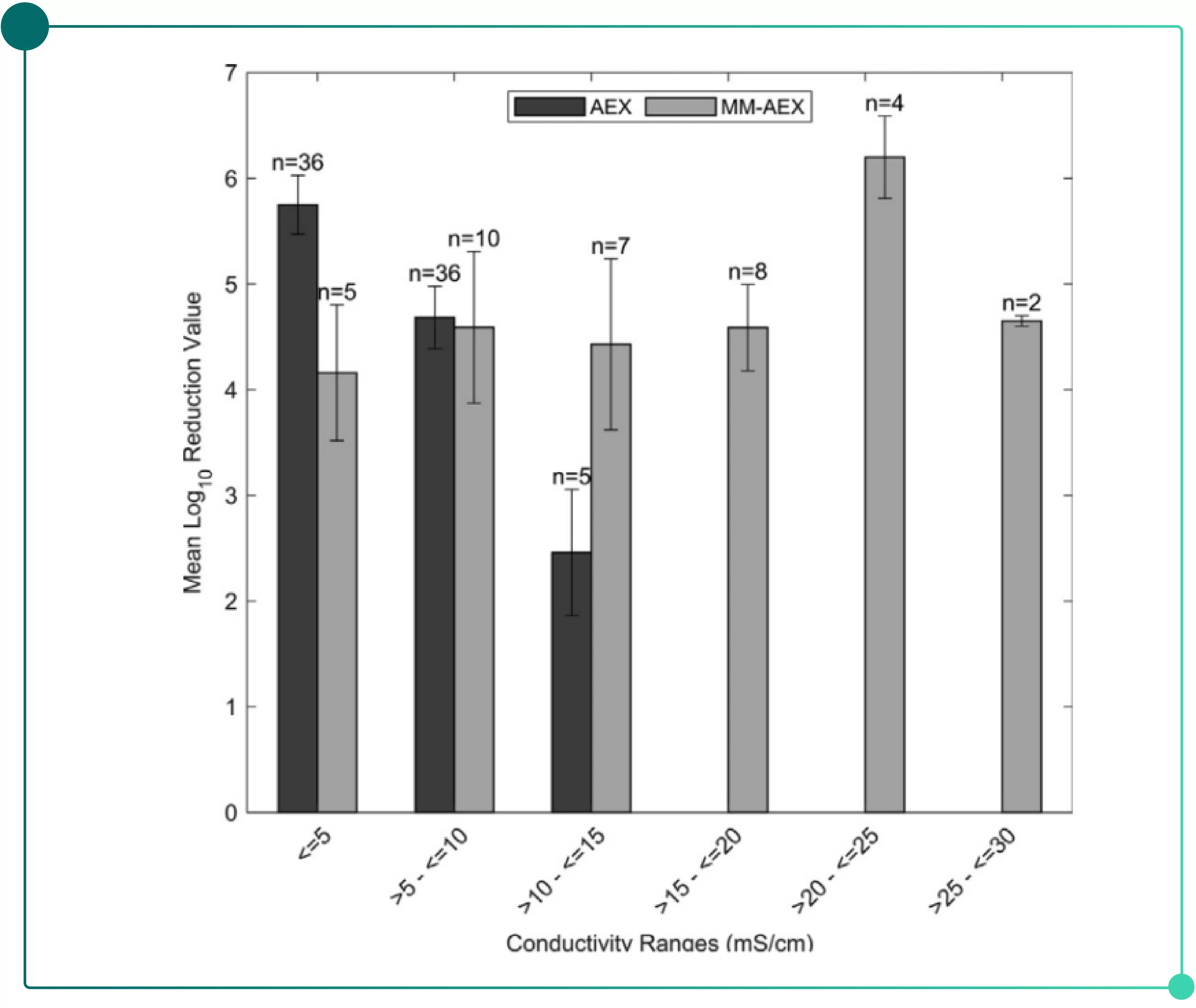
Fig.2 復合模式陰離子層析 vs. 單一陰離子層析對細小病毒的去除能力比較(FDA數據庫統計)
AEX病毒去除能力的關鍵影響因素病毒-介質相互作用強度可能受到病毒等電點(pI)與溶液pH值、溶液鹽濃度、Mab性質、病毒上可用結合位點的數量以及競爭物存在等因素相互作用的的影響。
? pH值:病毒-AEX的相互作用為靜電,但在低鹽條件下,X-MuLV在不同pH下清除效果比較穩定,X-MuLV和AEX填料之間的相互作用在5.0~8.0的范圍內僅略微依賴于pH值。與X-MuLV 清除率不同,不同pH值的MVM(pI 6.2)去除符合預期,當50 mM氯化鈉的pH值從5增加到8時,LRV大約增加4。
? 離子強度:對于單一的陰離子層析,通常隨著鹽濃度增加,病毒去除效果逐漸降低。而復合模式層析受鹽濃度影響較小,由Fig.2可知。
? Mab性質:對于任何給定類型的色譜分析,特定病毒的清除率不僅受色譜形成條件的影響,還受目標mAb本身的影響,病毒可以通過其表面負電荷與帶正電荷的mAb相互作用,從而影響病毒的去除效果。
? 病毒種類:X-MuLV的pI為5.8,該現象(X-MuLV在pH值為5時與AEX介質結合)是不正常的,表明該病毒在該pH值時其表面仍舊含有帶負電荷的斑塊。可知pI是預測病毒等大型復雜結構與離子交換(IEX)填料相互作用是不足的。相反,在確定病毒-IEX 填料相互作用方面,病毒表面電荷分布比 pI 更相關。
綜上可知,陰離子層析對病毒的去除效果受到多種因素影響,因此為獲得穩健的病毒清除效果,單一模式陰離子層析建議pH 值為7.0~8.5、電導率<10 mS/cm和載量<100 mg/ml。
博格隆陰離子填料病毒去除能力數據 復合模式陰離子填料 Diamond MIX-A? 高效清除能力:在某項目中,針對多種包膜和非包膜病毒模型(X-Mulv, MVM, PRV, Reo3)Diamond MIX-A展現出優異的清除能力,LRV范圍達4.5-5.34 log。
? 卓越耐鹽性:在極具挑戰性的高鹽條件下(上樣電導22 mS/cm, pH 6.43, 載量~60 mg/mL),保留時間(5 min),Diamond MIX-A對X-Mulv仍實現了顯著的清除效果,LRV分別達到3.04 log、3.25 log,驗證了其在高鹽環境下的穩健性。
下表匯總了Diamond Q系列填料在多個單抗項目中對模型病毒X-MuLV和MVM的清除表現:
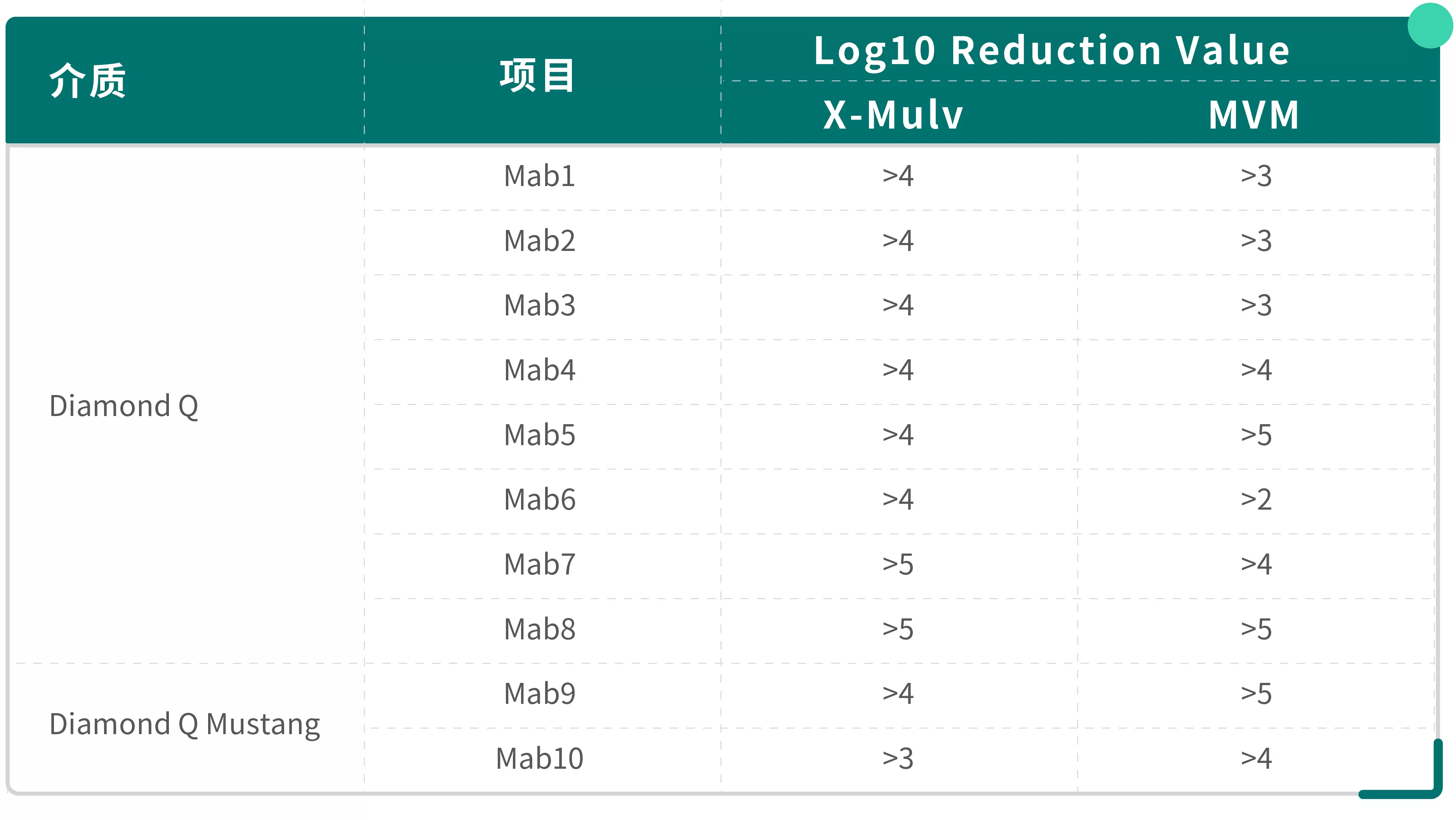
? Diamond Q對逆轉錄病毒X-MuLV展現出高度一致且優異的清除能力(所有項目LRV≥4 log)。
? 對細小病毒MVM的清除能力存在一定的項目間變異性(LRV范圍從2~5 log),這也印證了前文所述。盡管如此,在多數項目中仍能達到≥3 log的有效清除。
? Diamond Q Mustang 在測試項目中同樣表現出良好的病毒清除能力。
下游純化工藝中各層析步驟在病毒清除方面具有不同的能力和穩健性水平。陰離子交換層析(AEX),尤其是流穿模式(FT),已被廣泛證明是清除病毒的關鍵單元操作。
然而,即使是通常被認為穩健的AEX步驟,其清除效果(特別是對細小病毒)也可能因目標Mab的特異性、工藝參數的選擇而存在差異。復合模式AEX填料(如Diamond MIX-A)因其結合了多種作用力,在高鹽條件下展現出更穩健的病毒清除性能。
為確保病毒清除的穩健性,需在經過驗證的操作參數范圍內運行AEX。病毒清除研究應使用代表性的模型病毒,并在工藝最差條件的情況下進行,以充分證明該步驟在各種潛在風險場景下均能提供可靠且符合監管要求的病毒去除能力。
參考文獻[1] Barone, P.W., et al. Viral contamination in biologic manufacture and implications for emerging therapies. Nat Biotechnol 38, 563–572 (2020). (Updates the scope and context of viral risk).
[2] Ajayi, O.O., et al. An updated analysis of viral clearance unit operations for biotechnology manufacturing. Curr Res Biotechnol 4, 190-202 (2022). (Provides a modern overview of unit operations, including AEX).
[3] CAI, K., et al. Virus removal robustness of ion exchange chromatography. Biologicals 60, 64-70 (2019). (Specifically addresses robustness factors for IEX virus clearance, critical for the discussion on variability).
[4] Li, Y. Viral removal by column chromatography in downstream processing of monoclonal antibodies. Protein Expr Purif 198, 106131 (2022). (Focuses on chromatography for mAbs, directly supporting the application context).
關于博格隆
博格隆成立于2008年,是一家專注于為分離純化提供高質量層析介質的高新技術企業,是中國較早具備大規模生產分離純化介質能力的企業之一。博格隆所提供的產品涵蓋各類分離純化介質、預裝柱、實驗室及工業生產級空柱、微載體,同時提供分離純化工藝開發服務及填料定制。
本站“ABIO生物試劑品牌網”圖片文字來自互聯網
如果有侵權請聯系微信: nanhu9181 處理,感謝~





